🤝 アボガドロ定数・アボガドロ数とは(その違いも) 6. 結論からいいますと、標準状態においては空気1モルの体積=22. モル質量とは、その物質が6. 例えば固体炭素()についてみると、における昇華熱が 711. 高校生・受験生の多くは、 溶液の分野を苦手に思っています。

🤝 アボガドロ定数・アボガドロ数とは(その違いも) 6. 結論からいいますと、標準状態においては空気1モルの体積=22. モル質量とは、その物質が6. 例えば固体炭素()についてみると、における昇華熱が 711. 高校生・受験生の多くは、 溶液の分野を苦手に思っています。
アボガドロ定数・アボガドロ数とは(その違いも) 6. グラム毎モルは「一貫性のあるSI単位」ではないが、キログラム毎モルと同様にSI単位のひとつである。
しっかりと覚えておきましょう。

😛 定義から明らかなように、原子量 A r E と原子のモル質量 M E は実質的に同じものである。 なので、モル質量をよく理解し調べることは、 物質や粒子が何かを判別する 同定する 為に大切な情報の1つです。
この場合使われるのが、 molではなくてモル濃度になります。
Strauss『』 PDF 計量標準総合センター訳、、2009年、第3版。

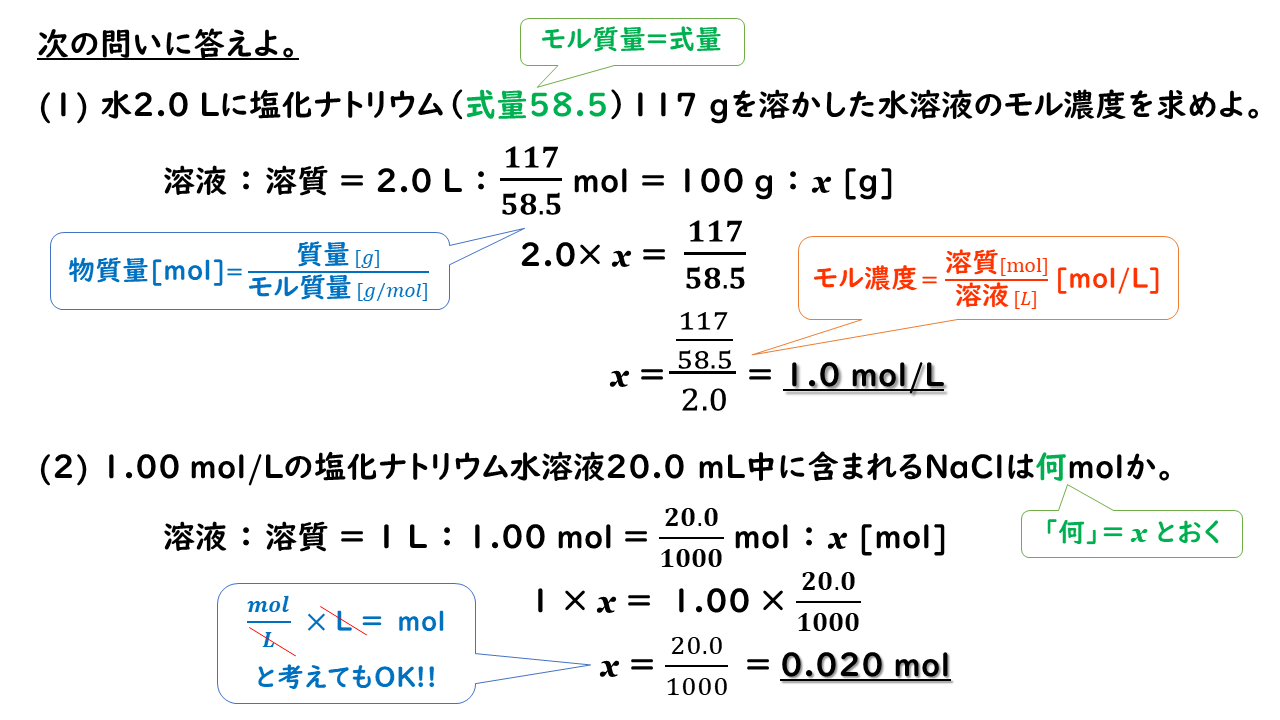
🖖 『』モル質量。 モル濃度とは モル濃度とは、溶質の物質量[mol]を溶液の体積[L]で割ったものです。 なんとなくは分かるのですが。
同じように、 原子の1個の重さも 元素 原子の種類 によって違います。

👍 (4)エチレン(C 2H 4)14gを完全燃焼させたときに生じる二酸化炭素(CO 2)の体積は何Lか。 それは、 molから何かの数値を求める時はかけ算を使い、反対に何かからmolを求めるのなら割り算を使うということです。 物質量とは原子の量でもあります。
10A ベストアンサー まず、全部 積分定数Cが抜けています。
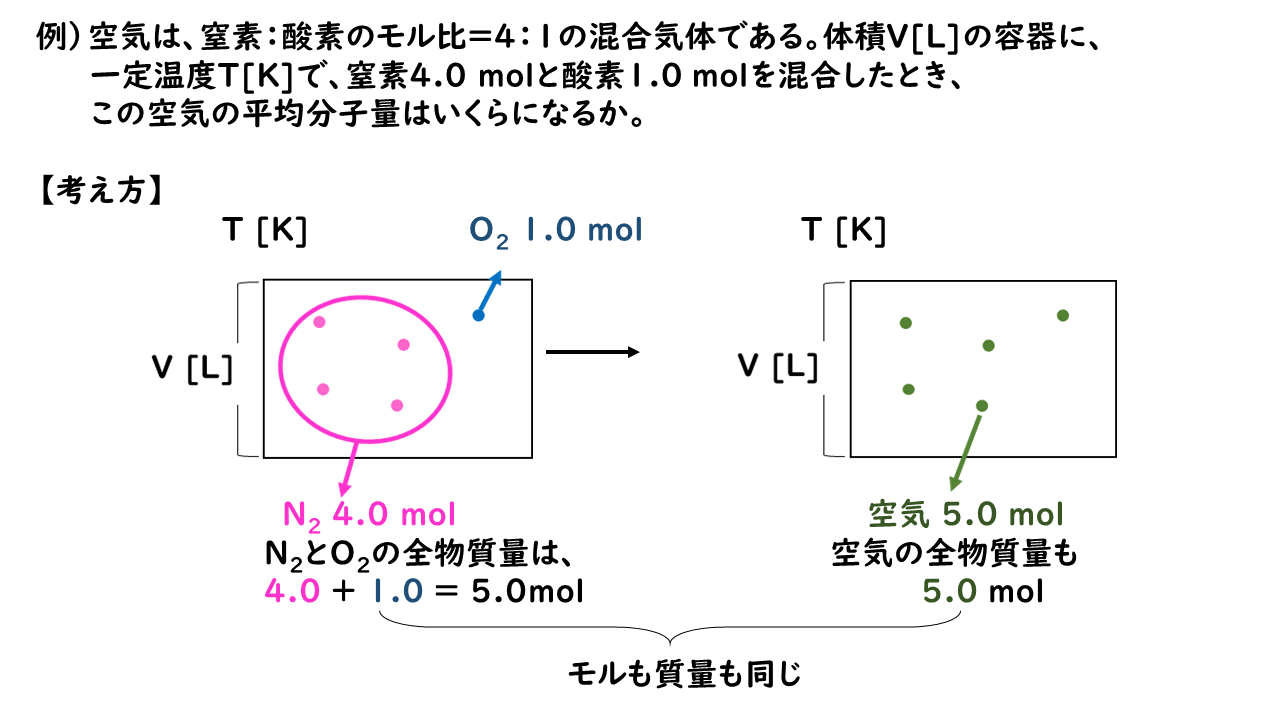
😘 混合物のモル質量 [ ] 複数の純物質の混ざり合ったでは、数平均モル質量 M n が定義される。 0molの空気の中には、窒素と酸素がそれぞれ何L含まれているか? ほとんどの場合、500mlといったように単位が違う形で出題されますので、まずは単位をLに直しましょう。
7濃硫酸側 溶質(硫酸分子)のモルを表したいです。
同じ元素の原子でも、により原子質量は異なる。