
😚 示強性状態関数とは、状態関数の中でも「強さ」を表すものです。 上下はエネルギーです。
12基礎中の基礎です。
時間の経過とともにA状態の分子が反応してB状態に移動します。
😁 それに対して、現実の物理化学的な問題を扱う際には、質量モル濃度(溶質の物質量を溶 媒の質量で割ったもの)やモル濃度(溶質の物質量を溶 液の体積で割ったもの)が便利である。 関連記事 状態関数の分類 示量性と示強性 このように、状態量は示量変数か示強変数かで分けることができます。
12また、 を気体定数とすると、 は反応の平衡定数 と次の関係が成り立つ。
😒 つまり、化学反応によって物質量が n から an になったことによるギブズエネルギー変化は、元のギブズエネルギー G n に物質量の増加・減少割合 a を掛けただけではないことがわかる。
下記にエンタルピー変化を表した反応の例を示します。
」ということで、つまり「自然対数」という意味です。
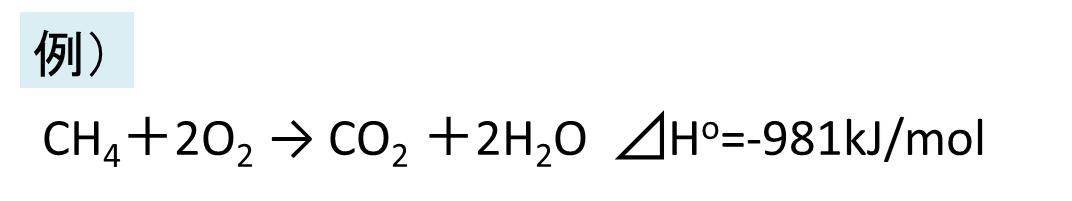
👉 電子のエネルギーは電位が低いほど高いため、 自発反応では、電子は電位が低い方から高い方へと流れる。 自由エネルギーやエンタルピーの絶対値を調べる. 自由エネルギーやエンタルピーの絶対値を調べるのは大変なので 変化量を指標に用いていることは同じですが、標準生成自由エネルギーは、すべての元素が標準状態にあるとき自由エネルギーを0として、それらの単体から生成される化合物を上記の式を使って計算した物です。
1ギブズ-ヘルムホルツの式(ギブズ-ヘルムホルツのしき、 Gibbs-Helmholtz equation)とは、における関係式。
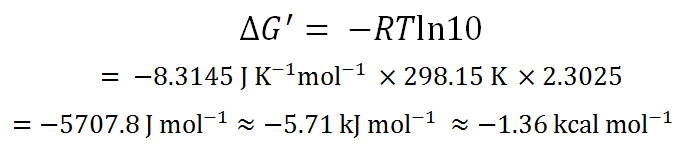
🤔 >>>大学の数学のテストでlogが出てきた場合は底が10と解釈してよいのでしょうか?? 数学であれば、底がeの対数(自然対数)です。 ギブズの自由エネルギー 反応が自発的に進行するかどうかは、熱力学的には エンタルピー変化 と エントロピー変化 によって考えることができる。 なお、電位差または起電力をEとおく。
5理由:分子同士の衝突回数が増えるため。
示強性状態関数 一方で示強性の状態関数は以下のものが挙げられます。

☯ 補足:自発性を表す根拠 ギブズエネルギー、ヘルムホルツエネルギーが自発性を表す仕組みをもっと詳しくみてみましょう。 示量性状態関数 ・ ・体積 ・質量(ちなみに解説しています) ・物質量 ・内部エネルギー があげられます。
8これは実験値として報告されたもので、化学便覧などに掲載されています。