💓 濃塩酸 3: 1の体積比で混合したものはと呼ばれ、高いをもつため、やなど、酸に対する耐性の高い金属の塩類製造に用いられる。 。 ナトリウムイオンNa+ 先ほどと同じで、 Na+とCl -は結びつかないまま存在しています。

💓 濃塩酸 3: 1の体積比で混合したものはと呼ばれ、高いをもつため、やなど、酸に対する耐性の高い金属の塩類製造に用いられる。 。 ナトリウムイオンNa+ 先ほどと同じで、 Na+とCl -は結びつかないまま存在しています。
寒天は水をゲル化して実験をビジュアル化するものとして使われています。
しかし、このとき塩酸は多くの用途を持つ重要な化合物となっていたため、新たな製造法が開発された。
ただし、前述のように酸性系統の薬剤(市販品含む)と反応して塩素ガスを生成したり、エタノール(消毒用を含む)と反応して有害なクロロホルムを生成する事がある。
💕 先ほどと同様、 H +と OH -が結びついて水 H 2Oになります。
の水溶液にを通じて得られる。
次のような流れで覚えておきましょう。
だが、いつもそうなるとは限らないんだ。

😄 酸・アルカリとは… ・ 酸・・・電離して H +を生じる物質 ・ アルカリ・・・電離して OH -を生じる物質 という物質でした。 彼が発明した塩酸と硝酸からなる金を溶かす液体、アクア・レギア(aqua regia、)はを捜し求める錬金術師たちに貢献した。
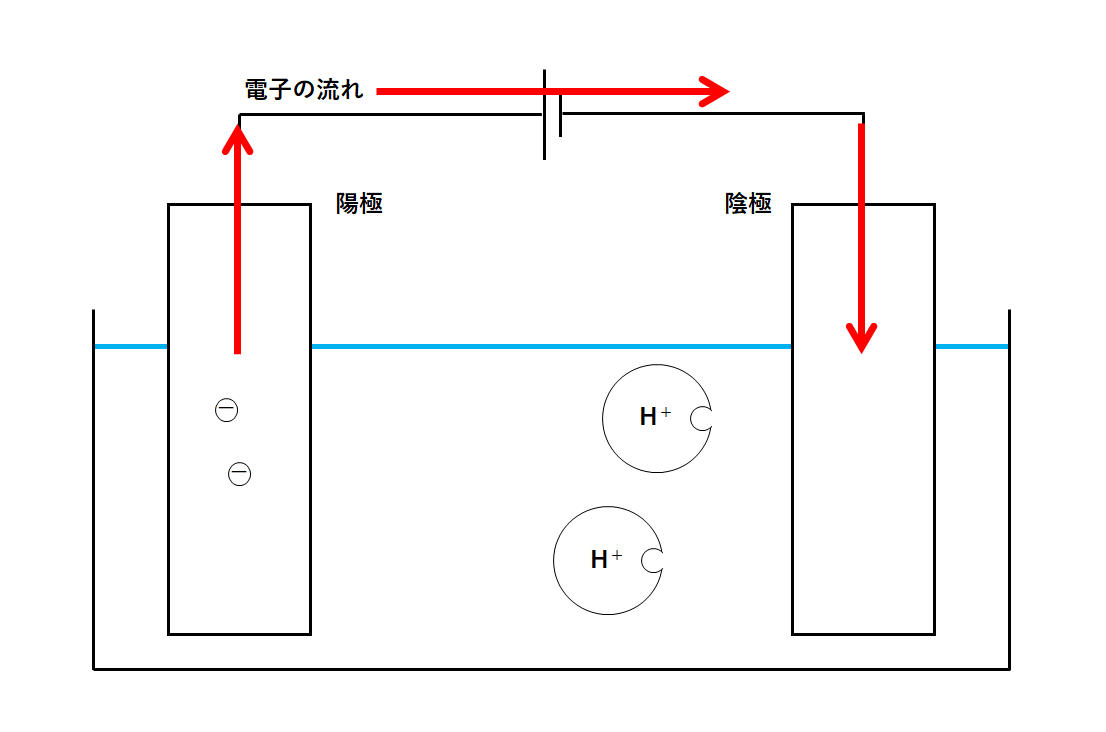
H 2Oに変化していく 塩化物イオンCl- Cl -は Na +と結びついて塩化ナトリウム NaClになる………ように思えます。
(つまり 中和が起こった。