
☺ この方法では、感染性のウイルスを扱う必要はありません。 大阪の研究所やベンチャーも加わり、吉村洋文知事も「7月から大阪府内で治験を開始する」と意気込む。
5これから半年、宇宙での生活が待っている。

⚑ 国内では、主に10ほどのワクチンの開発が製薬会社や研究機関などで進められている。 これは、弱毒化したウイルスなどを使うワクチンとは異なり、ウイルスの遺伝子情報を体内に注入して、抗体を作らせようというもの。 com —— 確認できる範囲では大きな副作用はなさそうということですね。
13しかし、コロナワクチンが臨床試験開始後6ヶ月以内に入手可能になる可能性は低いです。
増田道明 獨協医科大学医学部 教授 反町理キャスター: つまり、新型コロナウイルスのタンパクを体内で作ることにより新型コロナウイルスの侵入時に体内で止めることができるため、事前の防御策になると。
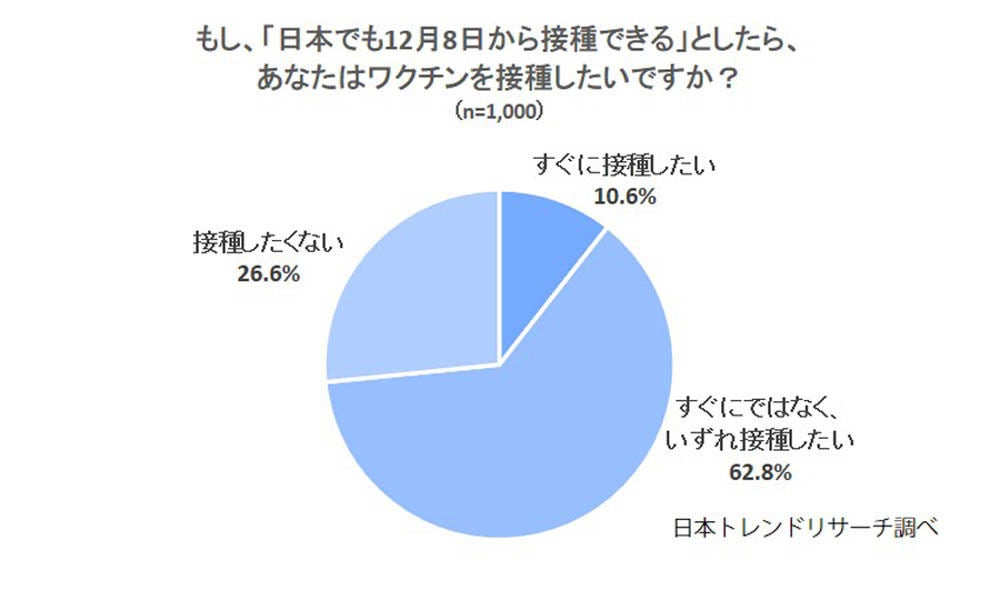
😙 優先順位としては、医療従事者は除いて、一般の人々では高齢者や基礎疾患がある人を優先的に接種していくようです。 日本人のCOVID-19の重症化に関わる遺伝子を特定 ワクチンを開発するために、COVID-19の重症化に関わる日本人特有の遺伝子を特定することが必要になる。
開発中のDNAワクチンでは、ウイルスの表面に見られる突起状の構造を作る遺伝子を導入したプラスミドを体内へ注入することを想定している。
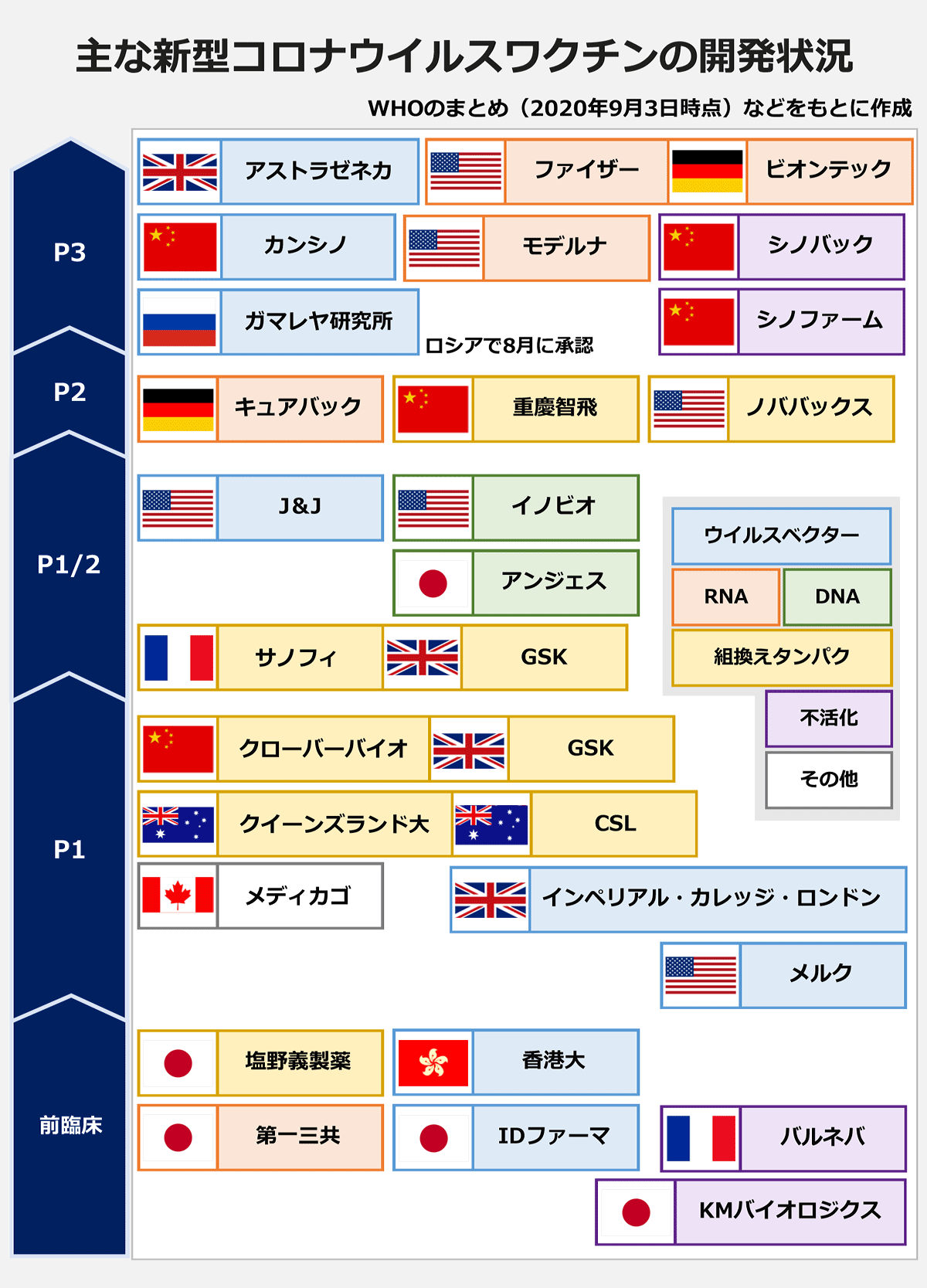
🤔 ワクチンの治験は国内初となる。 研究開発費は外部機関と共同で1000億円以上を投入し、アメリカの人口の3倍以上となる「10億回分を超えるワクチンを世界規模で供給する」と発表している。 (8月31日時点)。
8ウイルスそのものではないので病原性はなく、安全であるという利点もある。

💖 将来予測に関する表明 本プレスリリースには、モデルナ社が厚生労働省との間に締結する可能性のある供給契約に含まれる条件、武田薬品工業株式会社による流通、および合意に達した場合にはこの供給と流通の時期を含め、ただしこれらには限らず、1995年度米国民事証券訴訟改革法の意味の範囲内における将来予測に関する表明が含まれています。 抗ウイルス薬ではありませんが、独ベーリンガーインゲルハイムはCOVID-19による重篤な呼吸器疾患を対象に、TRPC6阻害薬「BI764198」のP2試験を10月に開始しました。
6臨床試験(第1相試験・第2相試験・第3相試験) 新しいワクチンを含む医薬品等の承認のためには、有効性・安全性等に関する科学的な見地からの審査が必要です。
一般的にワクチンの臨床試験では、同意を得た健康な希望者で安全性を確認する「第1相試験」、同意を得た少数の希望者で使用量や使用法、免疫反応を調べる「第2相試験」、同意を得た多数の希望者で有効性を調べる「第3相試験」を行います。