
⚓ ただし、冷却効率の面から見れば、断然食塩 NaCl の方が優れています。 12 とする。

⚓ ただし、冷却効率の面から見れば、断然食塩 NaCl の方が優れています。 12 とする。
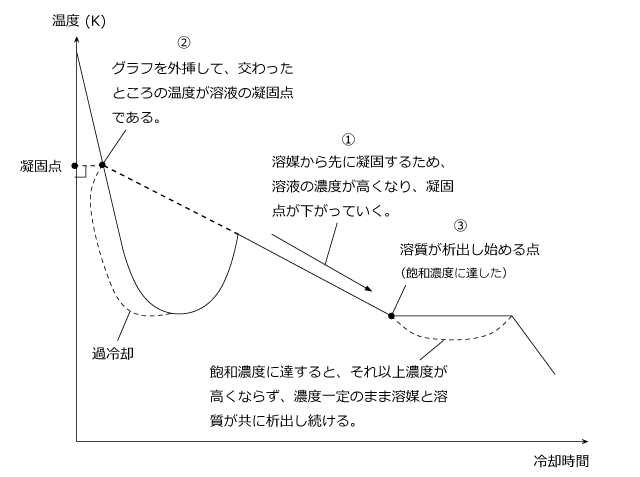
この冷却曲線から凝固点を読み取りますが、注意点があります。
⚔ ・異種分子間力>同種分子間力の場合 実在溶液の蒸気圧は、理想溶液の蒸気圧よりも小さい値を示す(負のずれ)。 凝固点降下度は何K になる 四塩化炭素のモル凝固点降下を29. この中で最も凝固点が低くなるもの、ア〜エの記号で答えなさい。
では沸騰とは何か? A「沸騰」とは、「飽和蒸気圧と大気圧が等しい時に液体中から蒸発し始める事」である。

😄 沸点上昇度・凝固点降下度の練習問題 では練習問題で慣れていきましょう。
凝固点降下の公式. i 液面差 h を水銀柱の高さに換算して求める 浸透圧の問題では、水銀 Hg の密度 13. どちらでもかまいません。

📱 こうして温度が低下すると、融解速度が低下して(融解速度は温度が高いほど大きい。
1 希薄溶液の束一性とは何か? 希薄溶液における「束一性 colligative properties 」とは、不揮発性溶質を含む希薄溶液の状態変化などに関する性質のことで、物質の種類あるいは性質によらず、濃度だけによって決定される性質をいいます。
まとめ 最後に沸点上昇、凝固点降下についてまとめておきます。

😒 水などの溶媒に塩化ナトリウムなどの不揮発性の溶質を加えると、つくった溶液の沸点は純粋な溶媒の沸点に比べて高くなる。 溶質は凝固しませんので、液体側は溶質が存在する分だけ凝固速度が遅くなります。 ここは自分でやるところです。
13よって、溶液は溶質粒子の種類によって、それぞれ異なる性質を示すようになり、その扱いは一層難しくなります。

😉 問題に与えられるので覚えなくても良いですけど、 「水のモル凝固点降下は 1. 密閉し容器内に適当量の水を入れて放置すると,その上部の空間に蒸発した水蒸気が,一定温度では一定の圧力を示すようになる。
18しかし、水溶液の蒸気圧は大気圧より小さくなるので、水溶液は沸騰しません。