
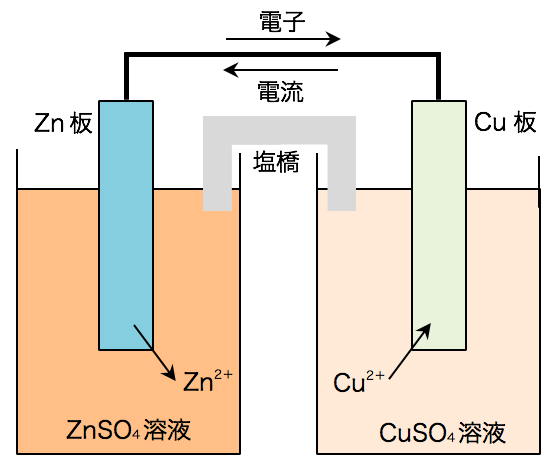
🤚 構造が単純なダニエル電池は、電池の基本を学ぶ教材として、頻繁に取りあげられます。
5実は時間が経つと電流が流れなくなってしまうのです。
電池の仕組み 「 電池」とは、 酸化還元反応で放出されるエネルギーを、 電気エネルギーとして取り出す装置 です。
次回は実用電池の燃料電池や鉛蓄電池について解説しようと思います。

😩 07Vです」 「ダニエル電池の起電力のほぼ2倍だね。 5ppmしか変化しない優れものだよ. それでいて,お値段が400円ときた.」 学生:「でも,5Vなんでしょう.1Vにしたいな.」 先生:「中学校で習った抵抗の直列繋ぎを応用して,同じ抵抗を5本つないで,1つの抵抗の両端で電圧は,5分の1になる.」 学生:「ふむふむ,思い出した.なんだぁ,それだかぁ.」 先生:「みなさんの先輩の今井直人くんが,を書いてくれたので,それを見ながら作ってください.」 先生:「このテキストを元に,大前くんが,」 大前:「ブレッドボードは繋ぎ方がわかんねーよ.どうつながっているの?テスターで導通確認をして使えばいいだよ.」 標準電池を使って電位差計を使った電位測定にトライしよう 先生:「これが標準電池だ。
そのため、イオンは素焼き板を通って亜鉛板に移動します 図4。
つまりダニエル電池では 負極側のイオン()が、正極側の硫酸イオン(陰イオン)に引き寄せられることによって、素焼き板をまたいでの移動が起こっています。
🌭 Aの方がイオン化傾向が大きいので、Bよりも先にイオンとなって溶液中に溶け出します。 つまり 亜鉛・・・(陽)イオンに なりたい 銅・・・・(陽)イオンに なりたくない というちがいが生じます。 」「ダニエル電池を長持ちさせるためには?」など、受験で頻出する問題を考えて解けるようになっているはずです。
この操作を精評と言う *本当に厳密に行う場合は、試料を乾燥させて水分を飛ばし重さが全く変わらなくなった重量を正しい質量とする。
銅は測定直前に研磨し、水で素早く洗浄する。
電解液を CuSO 4 水溶液にしたボルタの電池 しかし、実際にやってみると、Cu はZn よりもイオン化傾向が小さいので、Zn 板上で次の反応が起こり、Zn 板上にもCu が析出してしまいます。
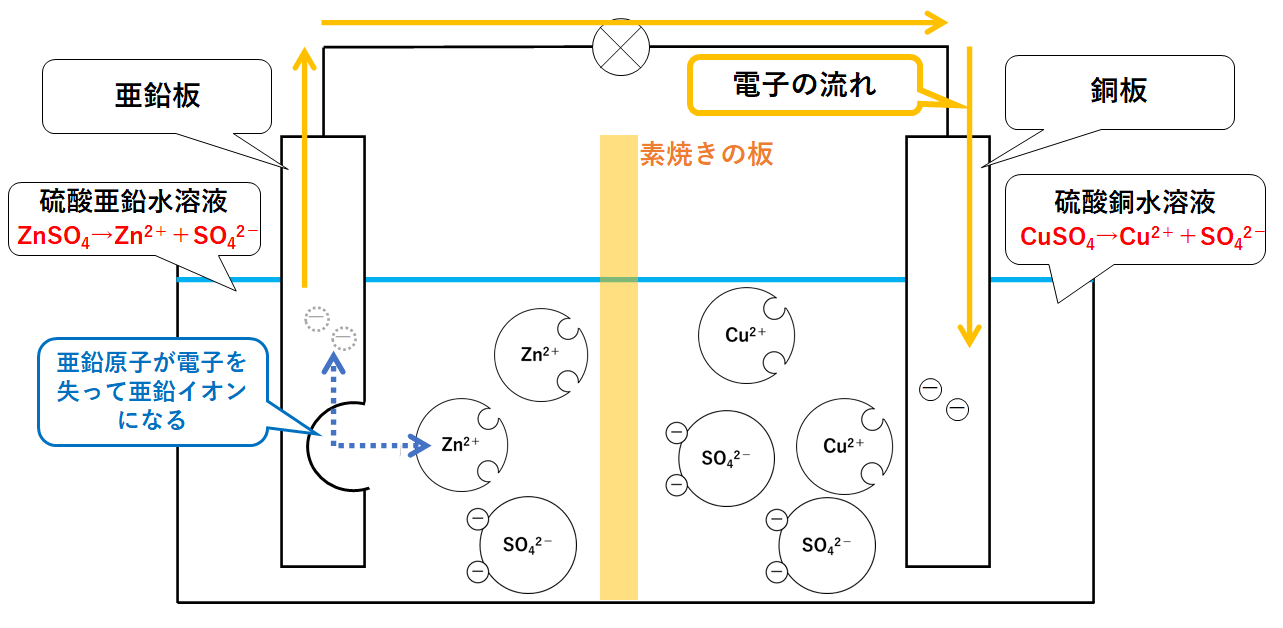
🚀 そのため、負極側は正に帯電し、正極側は負に帯電してしまい、すぐに電流が流れなくなってしまいます。 【参考実験動画】• つまり イオンの姿はいやだ、原子にもどりたいということです。 」 学生:「ICって,あのケータイ電話にはいっている四角に蠏さんの足がついているものね」 先生:「今回の心臓部は、REF02CPZで,精度が 5. 1836年、イギリスのダニエルは、+極と、-極を別々の溶液に浸けて、泡の発生を防ぐ方法を考え出しました。
1もし素焼き板がなく、適切ではないイオンの移動、すなわち、 正極側の銅イオンが負極側へ移動するような反応が起こったらどうなるでしょうか。